Aujourd’hui, l’implantologie est une discipline quotidienne en odontologie, accessible à l’omnipraticien, permettant de répondre à une demande croissante des patients pour des restaurations fixes et durables. D’après Lindquist et coll. (1), Roos et coll. (2), on constate un taux de survie élevée sur les dispositifs bénéficiant d’une maintenance en implantologie adéquate.
Avant toute chirurgie implantaire, un bilan parodontal doit être effectué ; la maladie parodontale doit être traitée et stabilisée. Cependant, si le taux de réussite des implants est aujourd’hui incontesté, leur durée de vie dépend néanmoins d’un entretien minutieux et d’une surveillance régulière. C’est pourquoi il est important d’effectuer une « maintenance implantaire ».
La maintenance parodontale et péri-implantaire reste en conséquence une étape essentielle du plan de traitement. Elle a comme objectif d’assurer à long terme la pérennité de nos traitements ; de prévenir les réactions inflammatoires des tissus mous (mucosite), les pertes d’attaches et les récidives de la maladie parodontale, les péri-implantites (Axelsson et coll., 3).
Nature des complications implantaires au cours de la maintenance
On peut observer deux types de complications :
- Les complications infectieuses : comme pour les racines des dents, les implants subissent des agressions externes (bactéries, aliments acides…). des pertes progressives des tissus autour de l’implant peuvent s’observer (péri-implantite). Ce phénomène infectieux est causé entre autres par un nettoyage insuffisant autour des implants.
- Les complications mécaniques : plus rares, ces complications peuvent être des fractures des implants eux-mêmes (col implantaire), ou des vis qui servent à fixer la prothèse dans l’implant.
Fréquence des séances de maintenance
Elle dépend des facteurs de risque du patient qui sont selon Heitz-Mayfield (4) : l’hygiène buccale, les antécédents des maladies parodontales et le tabagisme. Pour Axelsson et coll. (5), la fréquence des maintenances doit être de 2 à 4 fois par an. Une hygiène buccale inadaptée constitue un risque important dans le développement d’une affection péri-implantaire ; elle sera encore plus fréquente chez les patients fumeurs.
Antécédents de la maladie parodontale
Ils constituent un risque de développement d’une pathologie péri-implantaire. Axelsson et coll. (5) ont étudié sur 30 ans une population de 257 patients traités pour une parodontite chronique, puis suivis par des séances de maintenance : le niveau d’attache est stable sur plus de 95 % des sites. Seuls 3 % des sites ont une perte d’attache supérieure à 2 mm en 30 ans. Mais rappelons qu’en Suède, le suivi par des hygiénistes assure un niveau d’hygiène et de contrôle de la plaque bactérienne sans commune mesure avec des pays comme la France…
Montje et Coll (2016) (6), dans une revue systématique et une méta-analyse, aboutissent à des résultats très différents : les péri-implantites concerneraient 1 à 47% des implants.
L’ensemble de la littérature scientifique a démontré que les individus susceptibles à la parodontite sont plus exposés aux destructions péri-implantaires d’origine infectieuse. Roccuzzo et coll. (7), étudiant 101 patients atteints d’une parodontite chronique qui ont été traités et implantés, suivis sur dix ans, ont montré que les implants semblent plus susceptibles aux pertes d’attache que les dents.
Pour Pjetursson et coll. (8), les patients atteints de parodontite, présentant des poches résiduelles supérieures ou égales à 5 mm à la fin du traitement actif présentent un risque significatif de développement d’une péri-implantite autour des implants.
Tabagisme
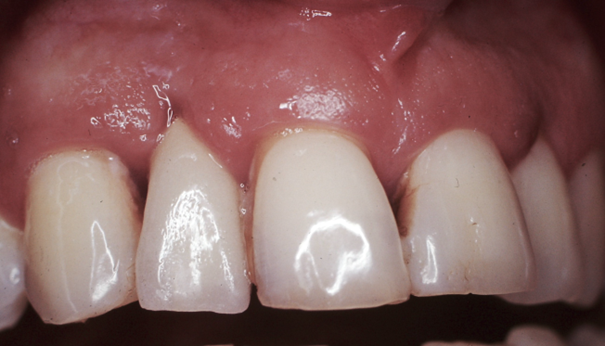
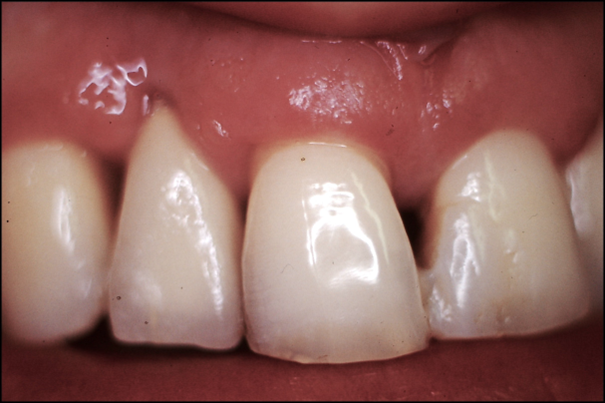
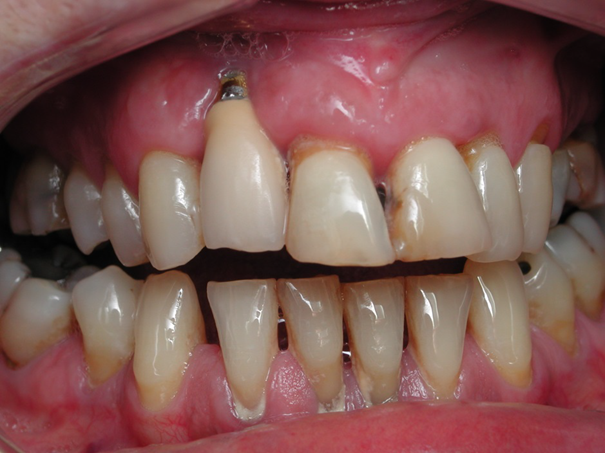
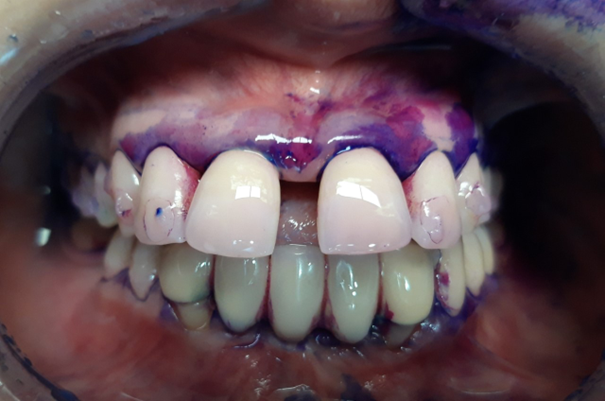
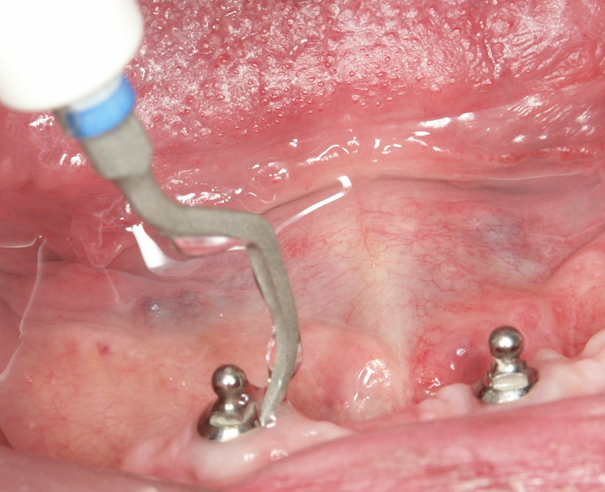
Il est démontré dans la littérature que les patients fumeurs sont plus susceptibles de développer une péri-implantite. Malgré tout, une bonne hygiène et un suivi régulier permettent d’assurer dans la majorité des cas une stabilité des tissus péri-implantaires (fig.1 et 2). Une négligence des maintenances régulières et ne hygiène inadéquate conduira inévitablement
à une péri-implantite (fig.3).
État de santé général
Tenir compte des pathologies d’ordre général notamment les maladies ou traitements immunodépresseurs ; le diabète non équilibré ; polyarthrite rhumatoïde, etc.
Le déroulement d’une séance de maintenance
Si la formation initiale des praticiens en implantologie n’a pas prévu d’aborder le sujet des échecs et des complications il est important de se renseigner auprès de confrères plus expérimentés ou de se former sur cet aspect de la discipline.
L’interrogatoire médical
Il vise à remettre à jour le questionnaire médical initial.
L’examen clinique
Il comprendra :
- La visualisation du biofilm à l’aide de colorants :
- Coloration directe passive : exemple : l’érythrosine (pastilles ou liquide), colorant rouge.
- Coloration différentielle : phloxine B (Papilli-plak test Gencibrosse) colorant les bactéries aérobies en rose et les anaérobies en bleu (fig 4 et 5).
- Coloration active : fluorescéine, révélant le biofilm en lumière bleue (système Flag for B Led Acteon).
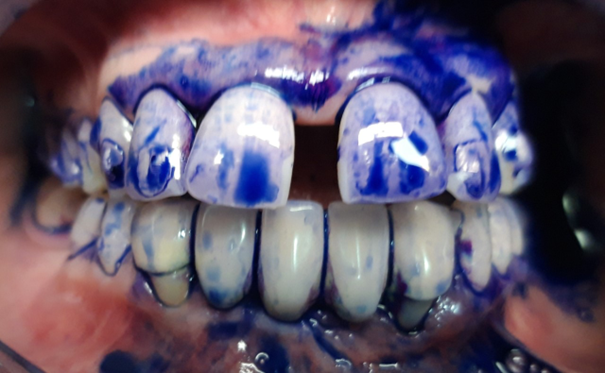
Ces colorants permettent également la mesure de l’indice de plaque du patient.
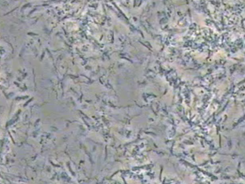
- Intérêt du microscope : Celui-ci permet de montrer au patient le biofilm et les bactéries mobiles, permet l’identification de plusieurs morphotypes et en particulier les spirochètes dans les maladies parodontales actives, permet de visualiser le rapport entre bactéries mobiles et non mobiles, de rechercher la présence de parasites (fig 6).
- L’examen du parodonte : Heitz- Mayfield et coll. (4), proposent l’utilisation d’outils de diagnostics ou d’examens essentiels lors de la maintenance :
- La sonde graduée en métal ou en plastique doit être utilisée avec une pression légère (0,25 N) pour le sondage des poches ; elle permet de diagnostiquer les maladies parodontales et péri-implantaires. La plus intéressante est certainement la sonde graduée UNCPCP15 de Hue Friedy (graduée tous les mm).
- L’augmentation de la profondeur de poche au sondage peut être associée à une perte d’attache et à une perte osseuse péri implantaire.
- La recherche du saignement au sondage, qui indique la présence d’une inflammation péri-implantaire.
- La suppuration est souvent associée à une perte osseuse péri-implantaire.
- La mobilité peut survenir lorsque la vis des structures prothétiques se dévisse. L’examen radiologique permet d’objectiver une perte osseuse péri-implantaire.
Nettoyage
Nettoyage quotidien du patient : Remotiver le patient et revoir la technique de brossage quotidien notamment au niveau des zones difficiles d’accès.
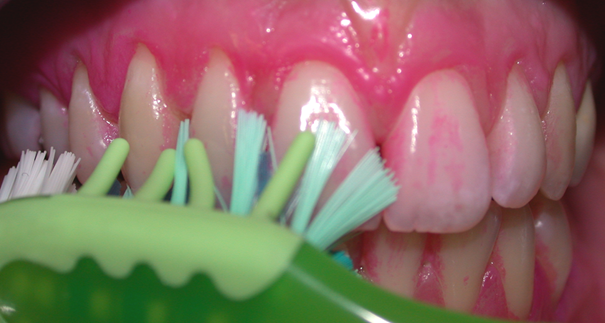
- Brossage quotidien, 2 à 3 fois par jour avec une brosse manuelle souple ou électrique, permet l’élimination du biofilm (fig 7).
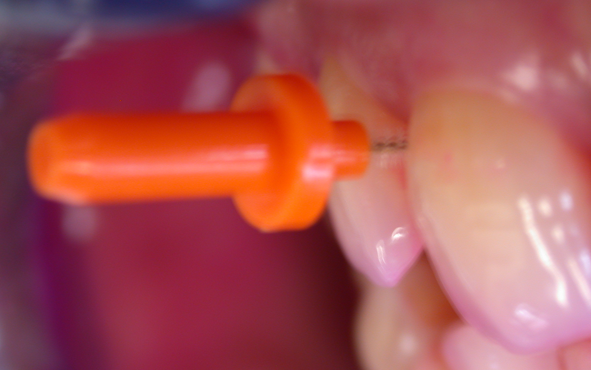
- Utilisation de brossettes interdentaires ou du fil dentaire pour le nettoyage des espaces interdentaires. Les brossettes doivent avoir une taille suffisante de sorte à pouvoir éliminer par friction le biofilm interdentaire (fig 8).
- Utilisation de brossettes monotouffes
- Utilisation du stimulateur gingival pour l’élimination de la plaque au niveau du sulcus. Prévenir le patient de ne pas arrêter le brossage en cas d’éventuels saignements, signes d’inflammation.
Nettoyage professionnel
- C’est l’élimination du tartre et du biofilm par le praticien : débridement des surfaces dentaires et implantaires grâce aux inserts montés sur ultrasons. L’objectif est d’éliminer le biofilm et/ou le tartre s’il y a lieu tout en préservant l’état de surface implantaire (Atieh et coll., 9). Utiliser plutôt des inserts en plastique pour le débridement des surfaces implantaires qui permettent une bonne élimination du biofilm, sans changer l’état de surface des implants (Speelmann et coll. 10) ; Schmage et coll. (11) observent cependant la présence de débris dus à l’usure de l’instrument.
- Le curetage et le surfaçage avec les curettes de Gracey se font de préférence avec des curettes plastifiées lors de la maintenance autour des implants, ou des inserts Titane Protect (fig 9).
- L’irrigation avec l’utilisation de bain de bouche, à 0,2 % de chlorhexidine, est efficace sur la réduction de plaque et de l’inflammation gingivale.
- L’aéropolisseur avec du bicarbonate de sodium en supra-gingival (Geursolley et coll. 12, Schwarz et coll. 13), de la glycine ou de l’Erythritol en sous-gingival, permet selon Tastepe et coll. (14), la suppression des endotoxines bactériennes dans 84 à 98 % des cas et l’élimination du biofilm à 100 %.
- La thérapie photodynamique enfin est une méthode efficace pour réduire la concentration bactérienne sur les surfaces implantaires (Marotti et coll. 15). À défaut, le polissage peut être réalisé avec des cupules ou brossettes et une pâte à polir.
Conclusion
De nombreuses études montrent des échecs implantaires chez les patients qui ne sont pas régulièrement suivis en maintenance (Pjetursson et coll. 8). La maintenance permettra de prévenir l’apparition de complications infectieuses autour des restaurations implanto-portées. C’est une étape importante et une obligation après le traitement implantaire, pour assurer la pérennité de nos traitements lors de la prise en charge de nos patients. Une information éclairée est indispensable, démontrant l’importance de leur implication quotidienne et du suivi une fois le traitement « actif » terminé.
Bibliographie
1. Lindquist, L.W., Carlsson, G.E. & Jemt, T. A prospective 15-year follow-up study of mandibular fixed prostheses supported by osseointegrated implants. Clinical results and marginal bone loss. Clinical Oral Implants Research 1996; 7: 329– 336.
2. Roos Jansacker AM, Renvert H, Lindahi C, Renvert S. Nine to fourteen year follow up of implant treatment, Part III : factors associated with peri implant lesions. Journal of clinical periodontology 2006 ; 33 : 296- 301.
3. Axelsson P., Nyström B, Lindhe J. The long term effect of a plaque control program on tooth mortality, caries and periodontal disease in adults. Results after 30 years of maintenance. J Clin Periodontol 2004 ; 31 : 749-7574
4. Heitz-Mayfield LjA : Péri implant diseases : diagnosis and risk indicators . J. Chir. Periodontal. 2008 : 35 (Suppl. 8) : 292 – 304.
5. Axelsson P, Lindhe J : The significance of maintenance care in the treatment of periodontal disease. J. Clin Perio 1981 ; 8 : 281 – 94.
6. A Monje, L Aranda , K T Diaz , M A Alarcón , R A Bagramian, H L Wang , A Catena.- Impact of Maintenance Therapy for the Prevention of Peri-implant Diseases: A Systematic Review and Meta-analysis. 2016 Apr;95(4):372-9.
7. Roccuzzo M, Bonino F, Aglietta M, Dalmasso P. Ten year results of a three arms prospective cohort study on implants in periodontally compromised patients. Part 2 :clinical results. Clin Oral Implants Res 2012 ; 23 : 389-395.
8. Pjetursson BE, Helbling C, Weber H.P, Matuliene G, Salvi GE, Brägger U, Schmidin K, Zwahlen M, Lang NP. Peri implantitis susceptibility as it releates to periodontal therapy and supportive care. Chir Oral Implants : Res 2012 ; 23 : 888-894).
9. M. A. Atieh, N. H. Alsabeeha, C. M. Faggion Jr., and W. J. Duncan. The frequency of peri-implant diseases: a systematic review and meta-analysis. Journal of Periodontology; 2012.
10. Speelmann J A, Collaert B, Klinge B. Evaluation of different methods to clean titanium abutments. A scanning electron microscopic study. Clin Oral implants Res. 1992 Sep ; 3 (3) : 120-7.
11. Schmage P, Thielemann J, Nergiz I, Scorziello TM, Pfeiffer P. Effects of 10 cleaning instruments of four different implant surfaces. Int Oral Maxillofac Implants. 2012 Mar-Apr, 27-2 : 308-17.
12. Geursolley J C. A meta analyses of six month studies of antiplaque and antigingivitis agents. J.Am. Dent. Assoc 2006 ; 137 : 1657-1657. 12. F.
13. Schwarz, D. Ferrari, K. Popovski, B. Hartig, and J. Becker. Influence of different air-abrasive powders on cell viability at biologically contaminated titanium dental implants surfaces. Journal of Biomedical Materials Research 2009; Part B, vol. 88, no. 1, pp. 83–91.
14. C. S. Tastepe, R. van Waas, Y. Liu, and D. Wismeijer. Air powder abrasive treatment as an implant surface cleaning method: a literature review. The International Journal of Oral & Maxillofacial Implants; 2012; vol. 27, no. 6, pp. 1461–1473.
15. J. Marotti, P. Tortamano, S. Cai, M. Simões Ribeiro, J.E. Miranda Franco et T.T. de Campos. Decontamination of dental implant surfaces by means of photodynamic therapy. Lasers Med Sci 2013; 28:303–309

